SÂM TAM THẤT
Ngày đăng: Ngày 30 tháng 6 năm 2025
SÂM TAM THẤT (Panax notoginseng)
Sâm tam thất dùng làm thuốc được ghi đầu tiên trong sách Bản thảo cương mục, tập 12 với tên Tam thất (Tianqi), còn có tên khác là Kim bất hoán, Điền thất (tienchi ginseng), Sơn thất (mountain plant), Nhân sâm tam thất (three-seven root), là rễ phơi khô của cây Tam thất (Panax notoginseng (burl.) F.H. Chen, hoặc Panax repens Maxim, hoặc Panax pseudoginseng var. notoginseng (Burkill) G.Hoo & C.L.Tseng, thuộc họ Ngũ gia bì (Araliaceae).
Các bộ phận của Sâm tam thất (P. notoginseng) hiện đang được ứng dụng rộng rãi trong ngành dược phẩm, bao gồm:
- Rễ và thân rễ Sâm tam thất (Notoginseng radix et rhizoma hoặc Radix Panasis notoginseng hoặc Sanqi (Sanchi) hay Jiankou): Đây là bộ phận được dùng nhiều nhất của cây.
- Rễ phụ Sâm tam thất: Panax notoginseng lateral roots / fibrous roots, rễ con (Jintiao).
- Nụ hoa Sâm tam thất: Panax notoginseng flower buds.
- Lá Sâm tam thất (Panax notoginseng Folia).
- Hạt sâm tam thất: Panax notoginseng seeds.
Tính vị quy kinh:
Vị ngọt, hơi đắng, tính ôn. Qui kinh: can, vị.
- Theo Y văn cổ:
Theo sách Bản thảo cương mục: “ngọt, hơi đắng, ôn, không độc”.
Sách Bản thảo hội ngôn: “vị ngọt hơi đắng, tính bình, không độc, qui dương minh quyết âm kinh”. Sách Bản thảo bị yếu: “ngọt, đắng, hơi ôn”. Sách Bản thảo cầu chân: “nhập can, vị kiêm tâm, đại tràng”. Sách Bản thảo tái tân: “nhập phế, thận”.
Thành phần chủ yếu
Do cùng thuộc chi Nhân sâm (Panax) nên ba loài: Nhân sâm Hàn Quốc (Panax ginseng), Tây dương sâm (Panax quinquefolius) và Sâm tam thất (Panax notoginseng) chia sẻ nhiều đặc điểm chung về hình thái và thành phần hóa thực vật. Tuy nhiên, mỗi loài vẫn sở hữu những đặc trưng riêng. Dưới đây là bảng phân tích so sánh các khác biệt về hóa thực vật giữa chúng:
Nhóm saponin triterpens (Ginsenosides):
|
Thành phần hoá học |
SÂM CAO LY Panax ginseng |
TÂY DƯƠNG SÂM (Panax quinquefolius) |
SÂM TAM THẤT (Panax notoginseng) |
|
Saponin chính |
Protopanaxadiol (PPD): Rb1, Rb2, Rc, Rd, Rg3. Protopanaxatriol (PPT): Re, Rf, Rg1, Rg2, Rh1. |
PPD chiếm ưu thế hơn: Rb1, Rc, Rd, Rg3. PPT: Re, Rg1 (hàm lượng thấp hơn) |
PPD và PPT: Rb1, Rd, Re, Rg2, Rh1. Saponin đặc trưng: Notoginsenosides (R1, R2, R3, R4), C3, D1, D2, E2. |
|
Đặc điểm nổi bật |
Hàm lượng Rg1 và Rb1 cao. Tỷ lệ Rg/Rb cao (> 0.4) → tác dụng kích thích thần kinh. |
Hàm lượng Rb1 cao hơn Rg1. Tỷ lệ Rg/Rb thấp (< 0.4) → tác dụng làm dịu, thanh nhiệt. |
Notoginsenosides (đặc trưng) có hoạt tính cầm máu, chống viêm mạnh. Ginsenoside Rg1 hỗ trợ tuần hoàn máu. |
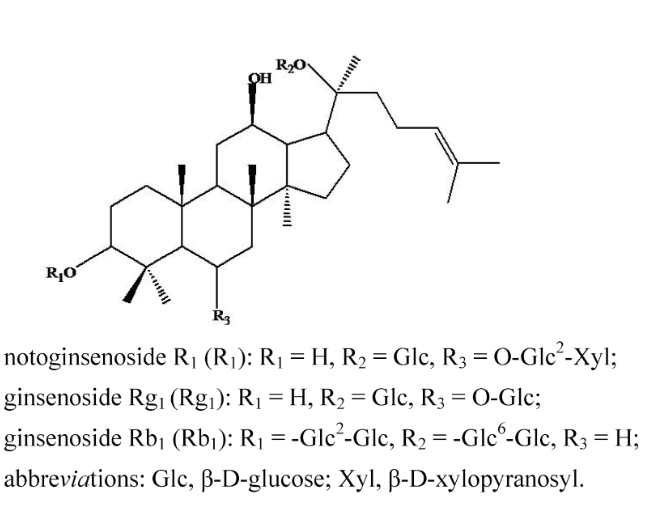
Nhóm hoạt chất đặc trưng:
|
Thành phần hoá học |
SÂM CAO LY (Panax ginseng) |
TÂY DƯƠNG SÂM (Panax quinquefolius) |
SÂM TAM THẤT (Panax notoginseng) |
|
Hợp chất nổi bật (độc đáo) |
Ginsenoside Rf (chỉ có ở Nhân sâm Hàn Quốc). |
Pseudoginsenoside F11 (đặc trưng của Sâm Bắc Mỹ). |
Dencichine (chất cầm máu mạnh). Notoginsenosides (R1-R4, C3, D1, D2, E2). |
|
Flavonoids |
Có, nhưng ít được nghiên cứu |
Có, hàm lượng trung bình |
Hàm lượng cao → hỗ trợ chống oxy hóa |
|
Phytosterols |
β-Sitosterol, Stigmasterol |
Tương tự Panax ginseng |
β-Sitosterol, Daucosterol |
|
Alkaloids |
Có, hàm lượng thấp |
Có, hàm lượng thấp |
Có, kết hợp với saponin tăng hiệu quả dược lý |
|
Tinh dầu |
Chứa α-Pinene, β-Elemene |
Chứa β-Caryophyllene, Limonene |
Rễ: α/β-Guaien, Octadecan Hoa: Elemen, Heptacosan, Pentacosan |
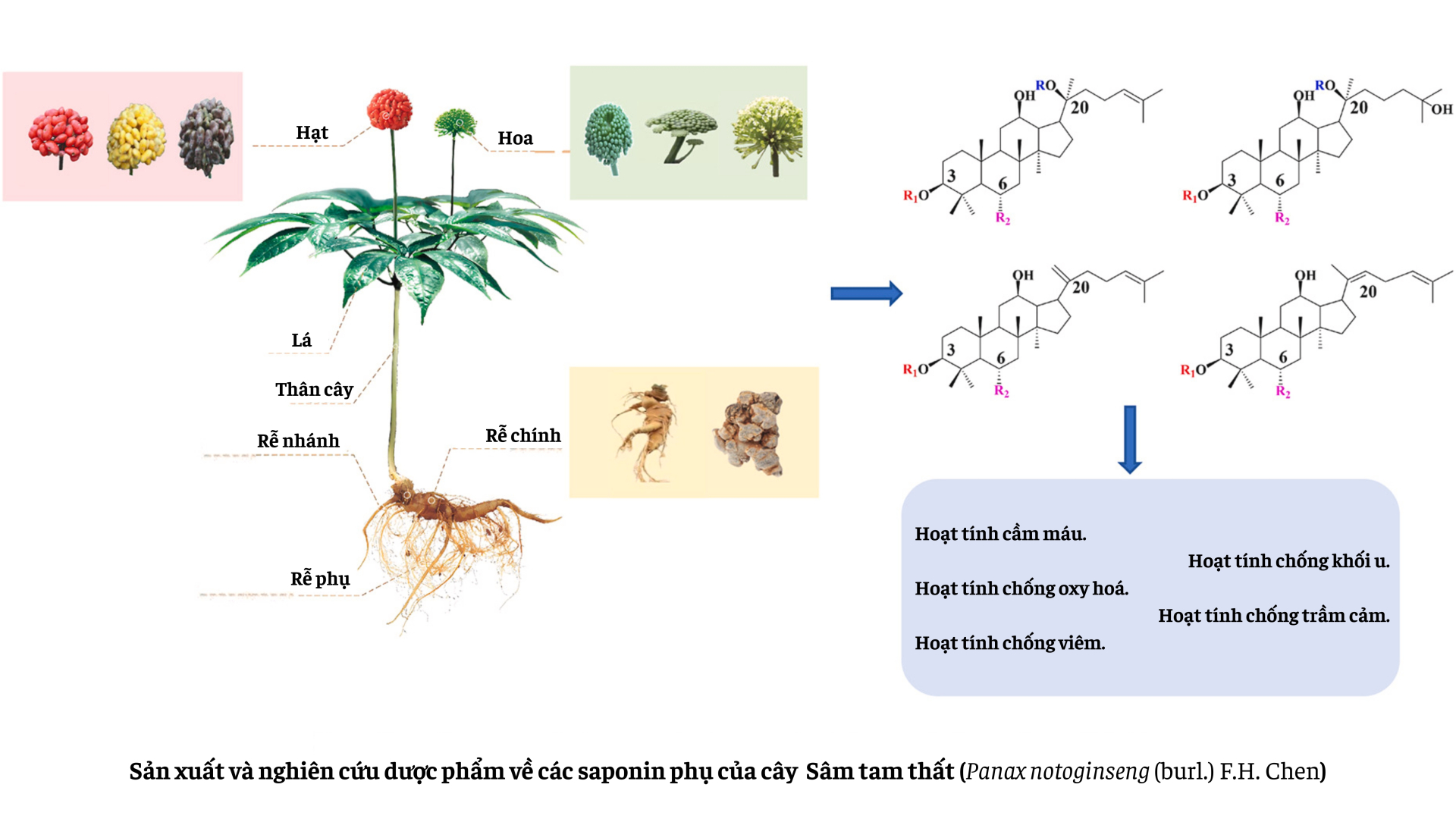 Mô tả sâm tam thất và đặc tính dược lý của cây (Source: Production and pharmaceutical research of minor saponins in Panax notoginseng (Sanqi): Current status and future prospects - ScienceDirect)
Mô tả sâm tam thất và đặc tính dược lý của cây (Source: Production and pharmaceutical research of minor saponins in Panax notoginseng (Sanqi): Current status and future prospects - ScienceDirect)
Kết luận: Sự khác biệt chính giữa Nhân sâm Hàn Quốc, Tây dương sâm, và Sâm tam thất nằm ở hồ sơ saponin và sự hiện diện của các hợp chất đặc trưng như ginsenoside Rf (Panax Ginseng), pseudoginsenoside F11 (Panax Quinquefolius), notoginsenosides và dencichine (Panax Notoginseng). Tỷ lệ Rg1/Rb1 cũng là một thông số quan trọng để phân biệt, với Tây dương sâm có tỷ lệ thấp hơn. Những khác biệt này giúp hiểu rõ hơn về đặc tính dược lý và ứng dụng của từng loài trong y học.
Các nhóm thành phần hoá học khác:
|
Thành phần hoá học |
SÂM CAO LY (Panax ginseng) |
TÂY DƯƠNG SÂM (Panax quinquefolius) |
SÂM TAM THẤT (Panax notoginseng) |
|
Polysaccharides |
Hàm lượng cao → tăng miễn dịch |
Hàm lượng trung bình |
Hàm lượng cao → kích thích miễn dịch và chống ung thư. |
|
Acid amins |
18–20 loại (chủ yếu arginine, glutamic) |
Tương tự Panax ginseng |
Đa dạng, bao gồm các acid amin thiết yếu |
|
Carotenoids |
Có, hàm lượng thấp |
Có, hàm lượng thấp (chủ yếu là β-carotene) |
Caroten (tiền vitamin A) cao hơn, hỗ trợ sức khỏe mắt và da |
|
Các khoáng chất |
Canxi, Sắt, Kẽm |
Canxi, Magie |
Canxi, Kali, Sắt |
Như vậy, Sâm tam thất (panax notoginseng), một loại dược liệu quý, nổi bật với các hợp chất đặc trưng như notoginsenosides và dencichine, mang lại khả năng cầm máu và chống viêm vượt trội. Nhờ cơ chế tác động đa chiều, Sâm tam thất không chỉ hỗ trợ điều trị các bệnh lý tim mạch mà còn giúp giảm đau hiệu quả, trở thành một ứng cử viên tiềm năng trong y học hiện đại. Đặc biệt, hàm lượng cao flavonoid và polysaccharide trong Sâm tam thất mở ra cơ hội ứng dụng rộng rãi trong lĩnh vực mỹ phẩm và thực phẩm chức năng, bởi khả năng chống oxy hóa, tăng cường miễn dịch và bảo vệ tế bào. Trong tương lai, Sâm tam thất hứa hẹn sẽ tiếp tục được khai thác sâu hơn trong các sản phẩm như: thuốc cầm máu, kem trị viêm khớp, và viên uống hỗ trợ tim mạch, góp phần nâng cao chất lượng cuộc sống và sức khỏe con người.
Theo Dược điển Việt Nam V, các hợp chất như ginsenoside Rg1, Rb1 và notoginsenoside R1 được sử dụng làm chất đối chiếu trong định tính và định lượng Sâm tam thất. Dược điển Trung Quốc 2020 cũng áp dụng phương pháp tương tự. Tương tự, Dược điển Mỹ và Anh 2024 cũng sử dụng ba hợp chất này trong phân tích Sâm tam thất.
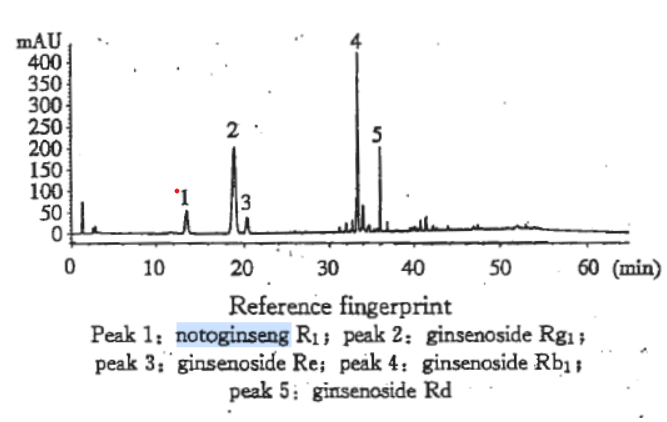
Sắc kí đồ HPLC đánh giá tổng lượng saponin của sâm tam thất đối với chất chuẩn đối chiếu (Source: Dược điển Trung quốc 2020)
Mặc dù notoginsenoside R1 và dencichine đều là những hợp chất đặc trưng quan trọng của Sâm tam thất, bởi chúng sở hữu cơ chế tác động và đặc tính dược lý khác nhau. Vì vậy, việc so sánh hai hợp chất này giúp làm rõ vai trò riêng biệt của từng thành phần trong tác dụng dược lý của Sâm tam thất (P. notoginseng), từ đó tối ưu hóa ứng dụng của dược liệu này trong điều trị các bệnh lý khác nhau. Dưới đây là bảng so sánh chi tiết, giúp làm sáng tỏ sự khác biệt giữa hai hợp chất:
|
Phân nhóm hợp chất |
Acid amin phi protein |
Saponin triterpenoid (khung dammarane) |
|
Công thức phân tử |
C5H8N2O5 |
C47H80O18 |
|
Khối lượng phân tử |
176.128 g·mol⁻¹ |
933.14 g·mol⁻¹ |
|
Công dụng chính |
Cầm máu mạnh, kháng viêm và bảo vệ chức năng thận. |
Bảo vệ tim mạch, kháng viêm, chống oxy hoá. |
|
Cơ chế tác động |
Ảnh hưởng đến quá trình đông máu, kết tập tiểu cầu và hệ thống tiêu sợi huyết. |
Giảm stress oxy hoá, kháng viêm, quá trình apoptosis thông qua con đường Akt/Nrf2. |
|
Độc tính |
Gây độc thần kinh ở nồng độ cao (ví dụ, gây bệnh thần kinh cơ (neurolathyrism) từ cây Đậu Lăng). |
Nhìn chung là an toàn, hiện tại chưa có báo cáo về phản ứng độc hại đáng kể. |
|
Phân bố nồng độ trong cây |
Nồng độ cao nhất ở rễ con (39.59%), sau đó là rễ chính (29.91%). |
Được tìm thấy tại rễ, thân, lá của Sâm tam thất. |
Tóm lại, từ bảng so sánh trên cho thấy, cả hai hợp chất đều có giá trị dược lý quan trọng nhưng với cơ chế tác động khác nhau:
- Dencichine được ứng dụng chủ yếu trong các trường hợp cần cầm máu, giúp rút ngắn thời gian chảy máu và tăng số lượng tiểu cầu.
- Notoginsenoside R1 có tiềm năng trong điều trị bệnh tim mạch và kháng viêm nhờ tác dụng bảo vệ mạch máu, chống viêm và chống oxy hóa.
*Sự thật về Dencichine trong rễ sâm Tam thất:
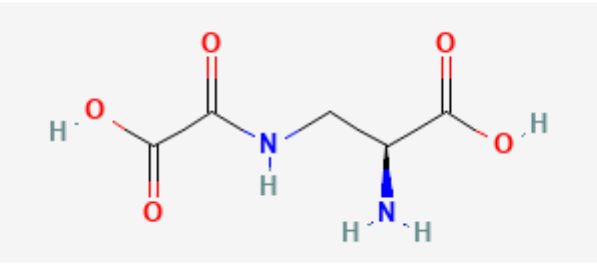
Hợp chất Dencichine (C5H8N2O5) (Source: Dencichin | C5H8N2O5 | CID 440259 - PubChem)
Dencichine (C₅H₈N₂O₅), đôi khi bị ghi nhầm thành “decichine”, là một acid amin phi protein đặc trưng của Sâm tam thất (Panax notoginseng). Hoạt chất này có tác dụng cầm máu, rút ngắn thời gian chảy máu, thúc đẩy quá trình đông máu và tăng số lượng tiểu cầu, đặc biệt hữu ích cho bệnh nhân giảm tiểu cầu do hóa trị. Đây cũng là một trong những thành phần chính của bài thuốc Bạch dược Vân nam (Yunnan Baiyao) – phương thuốc cầm máu nổi tiếng trong y học cổ truyền Trung Hoa.
Ngoài tác dụng cầm máu, nghiên cứu cho thấy dencichine còn giúp bảo vệ thận ở bệnh nhân tiểu đường, đặc biệt trong bệnh thận do đái tháo đường gây ra. Bên cạnh đó, nó có thể làm chậm quá trình mất xương, mở ra tiềm năng điều trị loãng xương ở phụ nữ sau mãn kinh. Dencichine cũng tác động đến phản ứng thiếu oxy của cơ thể, mang lại triển vọng trong điều trị các bệnh liên quan đến thiếu oxy.
Tuy nhiên, ở liều cao, dencichine có thể gây độc thần kinh, dẫn đến bệnh thần kinh cơ (neurolathyrism), gây liệt cơ và tổn thương hệ thần kinh trung ương. Tình trạng này thường gặp khi tiêu thụ quá mức thực vật chứa dencichine, như đậu lăng (Lathyrus sativus). Hiện nay, phần lớn nghiên cứu mới dừng lại ở mô hình động vật, cần thêm thử nghiệm lâm sàng để xác định mức độ an toàn trên người. Điều đáng chú ý là, dù dencichine có lợi ở liều thấp, nhưng khi dùng quá liều, nó có thể trở thành độc tố nguy hiểm cho hệ thần kinh.
Các nghiên cứu cũng đã xác nhận, dencichine có trong Sâm tam thất (P. Notoginseng), với nồng độ cao nhất lần lượt ở rễ con (39,59%), tiếp theo là rễ chính (29,91%), lá (16,21%) và thân (14,29%). Không có bằng chứng về sự hiện diện của dencichine trong Nhân sâm Hàn Quốc (P. Ginseng) hay Tây dương sâm (P. Quinquefolius), do đó đây là hợp chất đặc trưng của Sâm tam thất cho đến hiện nay.
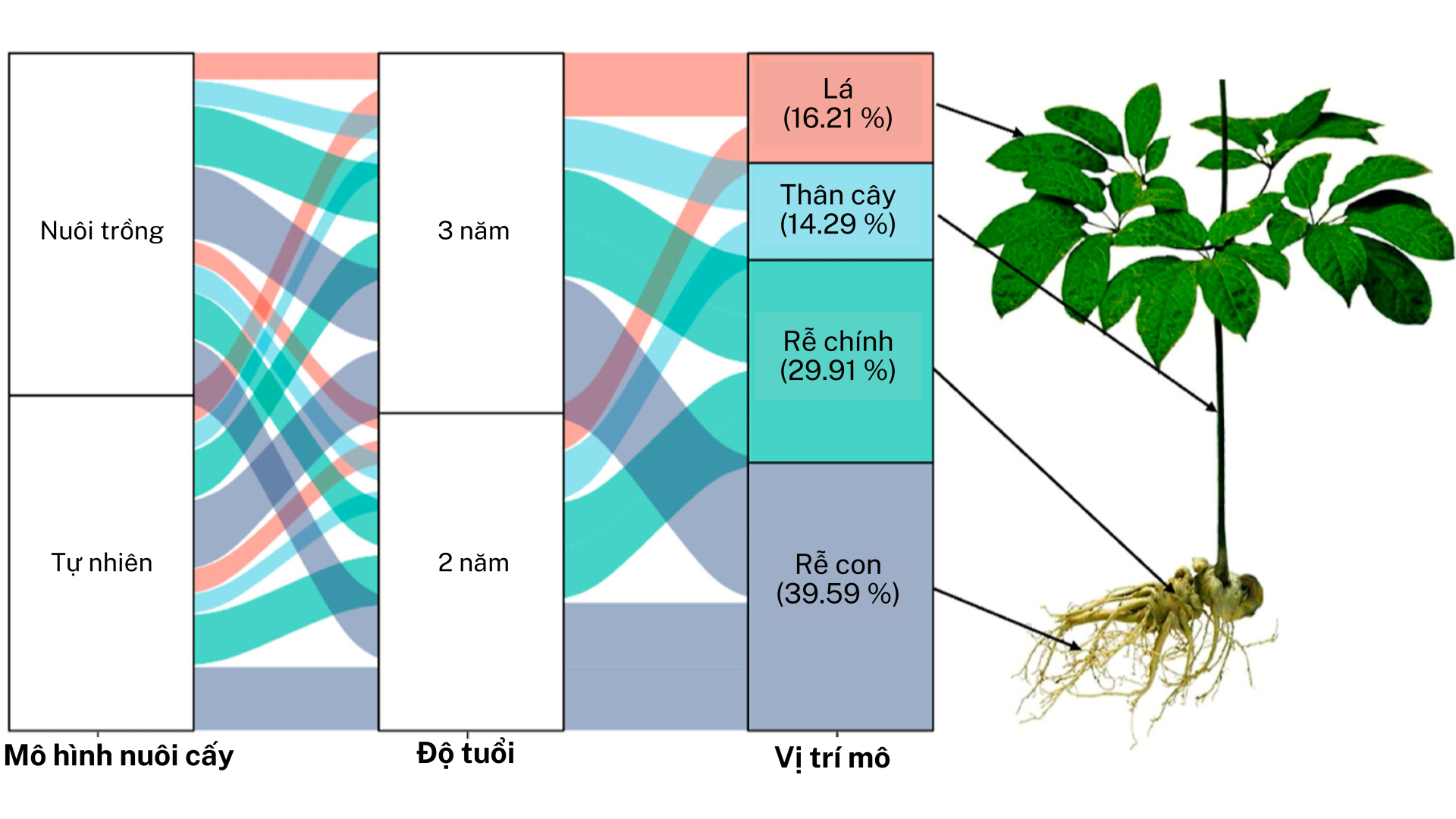
Sơ đồ Sankey cho sự phân bố của hợp chất Dencichines trong sâm Tam thất (P. notoginseng). (Source: Determination of Dencichine in Panax notoginseng in the Forest and Field Using High Performance Liquid Chromatography | ACS Omega)
Sự tích luỹ hợp chất Dencichine trong lá, thân, rễ chính và rễ con của Sâm tam thất (P. notoginseng) dưới các mô hình canh tác khác nhau. Kiểm định t được sử dụng để xác định mức độ ý nghĩa, ****(P < 0.0001), **(P < 0.01), và ns (P > 0.05). Soucre: Determination of Dencichine in Panax notoginseng in the Forest and Field Using High Performance Liquid Chromatography | ACS Omega
Tác dụng dược lý:
-
Theo Y học cổ truyền:
Hoá ứ chỉ huyết, hoạt huyết định thống, chủ trị các chứng xuất huyết ngoài và bên trong nội tạng, té ngã ứ huyết sưng đau.
Theo các Y văn cổ: Sách Bản thảo cương mục: “chỉ huyết tán huyết định thống, chảy máu do tổn thương dao kéo, té ngã, nhai nát hoặc tán bột bôi vào đều cầm máu, chủ thổ huyết nục huyết, hạ huyết, huyết lỵ, băng lậu, sau sách huyết ối không ra hết, đau do huyết ứ, mắt đỏ sưng mủ, hổ, rắn cắn chảy máu đều cầm”. Sách Y trung tham tây lục: “Tam thất vị đắng, hơi ngọt, tính bình, hoá ứ huyết chỉ huyết, vượng hành là vị thuốc chủ yếu cầm thổ huyết, nục huyết, bệnh khỏi không sinh ứ huyết ở kinh Lạc … kiêm trị nhị tiện hạ huyết, con gái băng huyết, lỵ ra máu đỏ tươi lâu không khỏi (nên cùng dùng với Nha đảm tử). Trường hợp ruột bị loét đi lỵ phân sắc tím hôi tanh có màng mỡ, loét ruột muốn thủng, Tam thất có tác dụng hoá hủ sinh tân, dùng để trị. Thuốc còn có tác dụng hoá ứ huyết trị chứng trưng hà, kinh nguyệt không thông, thuốc hoá ứ mà không hại huyết mới sinh, chảy máu ngoài da dùng bột đắp vết thương cầm ngay. Trường hợp té ngã tổn thương ảnh hưởng nội tạng kinh lạc đau ngoài đắp trong uống rất tốt. Nhọt mới bị sưng đau đắp ngoài là khỏi (nên kết hợp với đồng lượng bột Đại hoàng trộn dấm đắp). Trường hợp sang độc trong xương có thể dùng Tam thất làm độc thoát ra”.
-
Kết quả nghiên cứu dược lý hiện đại:
- Nhờ chứa các hợp chất saponin và polysaccharide, Sâm tam thất (P. notoginseng) sở hữu nhiều tác dụng dược lý quan trọng, bao gồm:
- Chống oxy hóa: bảo vệ tế bào khỏi tổn thương do gốc tự do.
- Tăng cường miễn dịch: thúc đẩy sản sinh IFN-gamma và TNF-alpha.
- Bảo vệ thần kinh: hỗ trợ tuần hoàn não, giảm tổn thương tế bào não trong tình trạng thiểu năng tuần hoàn.
- Tác dụng tim mạch: giúp điều hòa huyết áp, hạ lipid máu và ngăn ngừa huyết khối.
- Bảo vệ gan: giúp duy trì chức năng gan và chống lại tổn thương gan.
- Cải thiện sức khỏe mắt: hỗ trợ bảo vệ hệ võng mạc.
- Tác dụng nội tiết: hoạt động theo cơ chế tương tự estrogen, hỗ trợ cân bằng nội tiết tố.
Ngoài ra, các protein trong Sâm tam thất còn có đặc tính “kháng nấm”, đồng thời thể hiện hoạt tính enzym (ribonuclease, xylanase) và chứa trinolein – một triacylglycerol có tác dụng chống oxy hóa mạnh.
- Tác dụng cầm máu: Nước sắc uống của rễ Tam thất, bột Tam thất và dịch chiết nước Tam thất đều có tác dụng rút ngắn thời gian đông máu và thời gian Prothrombin có tác dụng ức chế ngưng tập tiểu cầu (theo Đoàn thị Nhu và Vũ Thị Tâm và Nguyễn Thị Thọ, Thông báo Dược liệu, 1977, 4, 14-20, Hà Nội) rễ Tam thất có khả năng kháng lại hiện tượng giảm Prothrombin trong máu thỏ và giảm khả năng máu đông gây thực nghiệm với Dicumarol. Một nghiên cứu vào tháng 3/2024 xác nhận rằng dịch chiết từ rễ Sâm tam thất, chứa dencichine và một số saponin, có tác dụng cầm máu rõ rệt, giúp rút ngắn thời gian đông máu cả trong và ngoài cơ thể. Đồng thời, nghiên cứu cũng chỉ ra rằng các hợp chất này có khả năng ức chế ngưng tập tiểu cầu ở một mức độ nhất định, tương tự như kết quả từ nghiên cứu tại Việt Nam. Trước đó, vào năm 2014, một nghiên cứu tiền lâm sàng đã chứng minh vai trò của dencichine trong việc rút ngắn thời gian chảy máu ở chuột, giảm thời gian thromboplastin một phần được hoạt hóa (APTT) và thời gian thrombin (TT), đồng thời làm tăng nồng độ fibrinogen trong huyết tương, qua đó hỗ trợ hiệu quả cầm máu một cách toàn diện.
- Ảnh hưởng của thuốc đối với trung khu thần kinh:
Saponin trong Sâm tam thất (P. notoginseng) có tác dụng đa dạng trên hệ thần kinh trung ương, tùy thuộc vào loại saponin:
- Saponin nhóm Rg có tác dụng kích thích thần kinh, giúp tăng cường tỉnh táo, chống mệt mỏi, cải thiện hiệu suất lao động trí óc và thể lực.
- Saponin nhóm Rb có tác dụng an thần, gây ngủ do khả năng ức chế thần kinh trung ương.
Thành phần saponin cũng phân bố không đồng đều trong cây: lá và hoa chứa nhiều saponin Rb nên có tác dụng ức chế thần kinh, trong khi rễ giàu saponin Rg, chủ yếu có tác dụng kích thích thần kinh. Đáng chú ý, tổng saponin từ cả rễ và lá đều thể hiện tác dụng giảm đau rõ rệt.
Ngoài ra, saponin Sâm tam thất còn mang lại lợi ích đáng kể trong bảo vệ thần kinh, đặc biệt ở bệnh nhân xuất huyết não giai đoạn đầu, giúp rút ngắn thời gian phục hồi. Nghiên cứu thực nghiệm cho thấy saponin có khả năng ức chế phù não, duy trì hàng rào máu-não (blood-brain barrier) và điều hòa biểu hiện protein quan trọng liên quan đến bệnh lý xuất huyết não, bao gồm tăng biểu hiện HSP70 (heat shock protein 70) và giảm biểu hiện transferrin.
- Ảnh hưởng của thuốc đối với hệ tim mạch:
- Hạ huyết áp và bảo vệ tim mạch: Dịch tiêm Sâm tam thất trên chó gây mê cho thấy tác dụng hạ áp, làm chậm nhịp tim, tăng lưu lượng máu động mạch vành và giảm lực cản mạch vành. Tổng saponin từ rễ Sâm tam thất giúp giảm huyết áp động mạch, giảm lực cản mạch máu ngoại vi, tăng cung lượng tim, đồng thời giảm tiêu hao oxy của cơ tim, có lợi trong bảo vệ tim khỏi tình trạng thiếu máu cục bộ.
- Tác dụng đối kháng với hormon tuyến yên: Chiết xuất rễ nhung của Sâm tam thất có khả năng đối kháng oxytoxin và vasopressin, đồng thời giảm rung tim do thiếu máu động mạch vành, góp phần ổn định hoạt động tim mạch.
- Bảo vệ tế bào cơ tim: Saponin trong Sâm tam thất có khả năng chống lại hoại tử cơ tim do angiotensin II, nhờ vào cơ chế giảm quá tải canxi nội bào, tăng hoạt động bơm canxi và giảm quá tải thất trái, giúp bảo vệ tim khỏi tổn thương do căng thẳng oxy hóa và rối loạn chức năng tế bào.
- Cải thiện tuần hoàn máu: Sâm tam thất còn có tác dụng giảm độ nhớt của máu, ức chế ngưng tập tiểu cầu và ngăn chặn sự hình thành huyết khối, từ đó tăng cường vi tuần hoàn mao mạch và cải thiện lưu thông máu, đặc biệt hữu ích trong các bệnh lý tim mạch và rối loạn tuần hoàn.
- Panaxydol chiết xuất từ Sâm tam thất ức chế sự phát triển của tế bào C6 gây u não và u tuỷ với ID(50) = 40 M, gây ức chế tế bào C6 sau 48 giờ.
- Dịch chiết hoa của Sâm tam thất có tác dụng hiệp lực với 5-fluorouracil (5-FU), một tác nhân hoá trị liệu các trường hợp ung thư đại tràng, trên khả năng ức chế sự tăng sản của dòng tế bào HCT-116 gây ung thư đại tràng ở người.
- Ginsenoside-R, notoginsenosid-R1, notoginsenosid-K và ginsenosid-Rh4, các saponin chiết xuất từ sâm Tam thất có tác dụng phá huyết nhẹ; kích thích sự tăng sản tế bào lách gây bởi concanavalin A (Con A), lipopolysaccharid (LPS), và ovalbumin (OVA); làm gia tăng các kháng thể đặc hiệu với OVA như IgG, IgG1 và IgG2b; làm gia tăng đáp ứng kháng thể với kháng nguyên OVA-Al(OH)3.
- Ảnh hưởng của thuốc đối với chuyển hoá: bột tam thất có tác dụng làm hạ Cholesterol, lượng Triglicerid trong máu. Saponin tam thất C1 có tác dụng điều tiết hai chiều đối với Glycogen tổng hợp và phân giải. Tổng Saponin của Tam thất có tác dụng thúc đẩy quá trình tổng bợp Protein huyết thanh của gan, làm tăng hàm lượng cAMP và làm giảm hàm lượng cGMP của tế bào cơ tim chuột nhắt, do đó mà làm tăng rõ rệt tỷ lệ cAMP/cGMP nhưng Tam thất nếu được chế biến với nhiệt độ cao ngược lại làm tăng cao cholesterol huyết thanh, Triglycerid, Betalipoprotein và làm giảm Alpha Lipo-protein.
- Sanchinosid C1 (ginsenosid Rg1) có tác dụng làm hạ đường huyết, hiệp lực với insulin trong thực nghiệm gây quá tải glucose.
- Dịch chiết nước, dịch chiết n-butanol và polysaccharid của sâm tam thất làm gia tăng sự di chuyển của tinh trùng. Ginsenosid-Rg1 trong Sâm tam thất có tác dụng nội tiết tố kiểu estrogen.
- Ảnh hưởng đến chức năng miễn dịch: Cũng như Nhân sâm, sâm Tam thất có tác dụng làm hồi phục lại bình thường phản ứng miễn dịch quá thấp hoặc quá cao không làm ảnh hưởng đến phản ứng miễn dịch bình thường của cơ thể.
- Dịch chiết nước từ Sâm tam thất làm giảm độ phù chân chuột gây bởi carragenin; ức chế sự tạo thành u hạt; ức chế chức năng của bạch cầu trung tính neutrophil; làm giảm sự hình thành gốc tự do superoxyd và ức chế sự sản sinh leukorien B4, nitric oxid (NO) và prostagladin E2 (PGE2). Cơ chế kháng viêm của sâm Tam thất có thể là do:
- Tác dụng ức chế hoạt năng của inducible NO synthase (iNOS) và cyclo-oxygenase-2 (COX-2); hoặc tác dụng ức chế hoạt năng của NF-kappaB và sự trình duyệt của tumor necrosis factor-alpha (TNF-alpha) mRNA.
- Tác dụng ức chế hoạt năng của phospholipase A2 (PLA2) và tác dụng ức chế sự gia tăng Neu-[Ca2+]i (hàm lượng canxi tự do trong nội bào của bạch cầu trung tính neutrophil).
- Độc tính của thuốc: Dùng liều chí tử chích tĩnh mạch thỏ nhà của cao nước Tam thất là 2.5-3 g/kg, chích ổ bụng chuột nhắt thì liều chí tử của mỗi loại chuột phân biệt là 0.5-0.75g/kg và 0.75-0.1g/kg. Tổng Saponin Tam thất tiêm dưới da chuột nhắt, LD50 = 1246 mg/kg, tiêm tĩnh mạch cho chuột nhắt LD50 = 628 mg/kg, 3-5% có tác dụng dung huyết nhẹ, tiêm tĩnh mạch cho 1ml 5% dịch Tam thất/phút thì liều chí tử là 587 108 ml/kg. Dùng bột Tam thất 15 g/kg cho bơm vào dạ dày chuột nhắt không có tử vong, sau 2 tuần, làm sinh thiết tim, gan, thận, lá lách, dạ dày và ruột đều không thay đổi.
- Một số kết quả nghiên cứu sâm Tam thất trên sức vật thí nghiệm của Đoàn Thị Nhu và cộng sự tại Hà Nội (Việt nam) (thông báo Dược liệu 1977, 4, 14-20, Hà Nội).
- Rễ Tam thất làm tăng khả năng hoạt động của súc vật thể hiện kéo dài thời gian của lô chuột thử thuốc so với lô đối chứng.
- Thuốc có tác dụng làm tăng sức đề kháng của súc vật đối với yếu tố độc hại như liều độc Uabain với tim, nhiệt độ môi trường xung quanh quá cao hoặc quá thấp vượt ngoài giới hạn điều hoà của cơ thể.
- Thuốc Tam thất khác với Nhân sâm không có tác dụng gây tăng huyết áp.
- Đối với tác dụng nội tiết:
- Rễ Tam thất thí nghiệm trên chuột cống cái non với liều 5 g/kg, uống trong 6 ngày đã làm tăng trọng lượng tử cung một cách có ý nghĩa so với lô chứng, chứng tỏ thuốc có tác dụng hướng sinh dục trên súc vật cái.
- Rễ Tam thất thí nghiệm trên chuột đực non với liều 5g/kg, uống trong 6 ngày, không làm thay đổi một cách có ý nghĩa trọng lượng tinh hoàn và tuyến tiền liệt so với chuột đối chứng, chứng tỏ Tam thất không có tác dụng hướng sinh dục đối với vật đực với liều này.
- So sánh hoạt tính gây động dục của rễ Tam thất có độ tuổi khác nhau, các tác giả có nhận xét là rễ Tam thất 5 năm có hoạt tính gây động dục hai lần mạnh hơn rễ Tam thất 3 năm.
- Nghiên cứu có tác dụng gây động dục của lá và rễ phụ so sánh với rễ củ Tam thất thì thấy lá Tam thất có hoạt tính yếu hơn khoảng 20 lần và rễ phụ có hoạt tính yếu hơn khoảng 8-10 lần so với rễ củ Tam thất 5 năm.
- Tác dụng tiêu viêm: Nước sắc Tam thất có tác dụng chống viêm đối với chuột cống gây viêm khớp thực nghiệm (ảnh hưởng của nước sắc Tam thất đối với viêm khớp thực nghiệm, Dược học báo 12: 446-451, 1965).
- Nước ngâm kiệt Tam thất trên ống nghiệm có tác dụng ức chế nhiều loại nấm ngoài da (Tạp chí Bệnh ngoài da Trung Hoa, 286-292, 1957).
- Tiềm năng điều trị ung thư:
Một nghiên cứu năm 2021 trên Frontiers in Pharmacology đã đánh giá chiết xuất từ Sâm tam thất trên nhiều dòng tế bào ung thư, cho thấy khả năng gây chết tế bào thông qua kích hoạt apoptosis, ức chế tăng sinh và ngăn chặn hình thành mạch máu mới (angiogenesis). Đặc biệt, nghiên cứu nhấn mạnh tiềm năng hỗ trợ điều trị ung thư đại tràng, gan và một số loại ung thư khác. Tương tự, một nghiên cứu năm 2009 trên PMC cho thấy chiết xuất từ rễ Sâm tam thất có thể tăng cường hiệu quả của các tác nhân hóa trị như 5-fluorouracil và irinotecan, làm giảm sự phát triển của tế bào ung thư đại tràng SW480. Những phát hiện này gợi ý khả năng hỗ trợ liệu pháp hóa trị, giúp giảm liều lượng thuốc cần thiết hoặc hạn chế tác dụng phụ, tuy nhiên, cần thêm thử nghiệm lâm sàng để xác nhận. Sau đây là bảng so sánh giữa 2 nghiên cứu trên:
|
Tạp chí nghiên cứu |
Loại ung thư |
Cơ chế |
Kết quả |
|
Đa dạng (nổi bật ở ung thư đại tràng, gan) |
Kích hoạt apoptosis, ức chế angiogenesis |
Hiệu quả trên dòng tế bào ung thư |
|
|
Đại tràng |
Tăng hiệu quả hóa trị, giảm tăng sinh |
Giảm sự tăng trưởng tế bào SW480 |
- Điều hoà vi khuẩn đường ruột:
Một nghiên cứu năm 2020 trên Phytomedicine đã chỉ ra rằng saponin từ Sâm tam thất có khả năng giảm béo phì ở chuột thông qua điều chỉnh hệ vi khuẩn đường ruột, thúc đẩy sinh nhiệt (thermogenesis) và tái cấu trúc tế bào mỡ nâu (beige adipocyte) qua con đường leptin-AMPKα/STAT3. Phát hiện này mở ra tiềm năng ứng dụng trong điều trị béo phì và rối loạn chuyển hóa. Tương tự, nghiên cứu năm 2024 trên tạp chí Journal of Functional Foods cho thấy Sâm tam thất giúp cải thiện sự phong phú và đa dạng của hệ vi khuẩn đường ruột, đặc biệt làm gia tăng Akkermansia spp., một loại vi khuẩn có liên quan đến cải thiện sức khỏe chuyển hóa. Những kết quả này gợi ý khả năng hỗ trợ điều trị tiểu đường và các bệnh lý chuyển hóa thông qua cơ chế tác động đến hệ vi sinh đường ruột.
- Tiềm năng hỗ trợ sức khoẻ tâm thần:
Một bài báo trên Frontiers in Pharmacology (2022) đã tổng hợp nghiên cứu trong 20 năm qua, nhấn mạnh rằng các thành phần hoạt tính của Sâm tam thất, đặc biệt là ginsenoside Rg1 và Rb1, có thể tác động đến các con đường liên quan đến trầm cảm thông qua điều hòa serotonin và dopamine. Bên cạnh đó, một nghiên cứu trên PMC mở rộng phạm vi đánh giá, cho thấy Sâm tam thất còn có tiềm năng hỗ trợ điều trị lo âu và suy giảm nhận thức nhờ đặc tính chống viêm và bảo vệ thần kinh, mở ra triển vọng ứng dụng trong các rối loạn thần kinh.
Ứng dụng lâm sàng:
- Trị các chứng xuất huyết:
- Dùng dịch tiêm sâm Tam thất trị xuất huyết đường tiêu hoá trên 110 ca, hiệu quả tốt hơn 50 ca đối chiếu dùng Tây Y. Số bệnh nhân bao gồm loét hành tá tràng 113 ca, viêm dạ dày mãn 19 ca, loét dạ dày 6 ca, loét hỗn hợp 4 ca, 18 ca chưa phát hiện bệnh lý.Tổ điều trị dùng dịch tiêm Tam thất do xí nghiệp 1 Thượng Hải sản xuất (2ml/ống hàm lượng 1g thuốc sống) (8-16ml) gia vào dung dịch Glucose đẳng trương 500 ml truyền tĩnh mạch ngày 1 lần, không dùng các loại thuốc cầm máu khác. Tổ đối chiếu 50 ca dùng Vitamin K và các loại thuốc cầm máu khác gia vào dịch Glucose đẳng trương, lượng và truyền như nau. Kết quả: Tổ dùng Tam thất máu trong phân chuyển âm tính bình quân sau 5.98 ngày, thời gian nằm viện trung bình là 15.2 ngày, tổ Tây Y, máu trong phân chuyển âm tính bình quân sau 9, 12 ngày và thời gian nằm viện trung bình 21.64 ngày (P nhỏ hơn 0.02 có ý nghĩa thống kê) (Phạm Xương Háo và cộng sự, Báo cáo 110 ca huyết xuất đường tiêu hoá trên chữa bằng dịch tiêm Tam thất, Tạp chí Trung Y Dược Thượng Hải 1983, 9:15).
- Trị xuất huyết bao tử: Dùng bột Tam thất mỗi lần 1.5g x 3 lần/ngày, uống với nước ấm, bệnh nhân nghỉ tại giường, trừ trường hợp nôn máu còn thì ăn bình thường, chế độ lỏng hoặc bán lỏng, sau khi máu phân âm tính còn uống thuốc thêm 2 ngày để củng cố. Kết quả 60 ca chảy máu khỏi hoàn toàn 58 ca, không khỏi 2 ca (La Dụ Dân, Bột điền thất trị xuất huyết bao tử, Tạp chí Trung Y Vân Nam 1985, 1:28).
- Trị loét dạ dày chảy máu cấp lượng nhiều: Hoà bột Tam thất 10g vào 30-50ml nước muối sinh lý, cứ mỗi 6-8 giờ bơm vào dạ dày 1 lần, kẹp ống trong 1 giờ rồi hút dịch dạ dày cho đến khi dịch không còn máu tưới, lưu ống dạ dày 2-3 ngày sau đó tiếp tục cho uống bột Tam thất mỗi lần 10g, 3-5 lần. Thời gian hết máu tươi trong dịch dạ dày từ 12 giờ (ngắn nhất) đến 96 giờ (dài nhất) bình quân 55.33 giờ, sắc phân trở lại bình thường 2-8 ngày, bình quân 3.83 ngày. Tác giả trị 6 ca, trừ 1 ca đã hết chảy máu và chết sau 5 ngày do viêm phổi và nhiễm trùng huyết, còn tất cả đều khỏi (Dương Quốc Phong, Trị dạ dày chảy máu cấp do loét, Thực dụng ngoại khoa tạp chí 1982, 4:90).
- Trị ho ra máu: Bột Tam thất mỗi lần uống 6-9g, ngày 2-3 lần, trị dãn phế quản, lao phổi và áp xe phổi kèm ho ra máu. 10 ca uống thuốc 5 ngày, cầm máu trong đó hoàn toàn cầm máu 8 ca, còn 2 ca cầm máu được 1-2 tuần lại ho ra máu ít (Trịnh Hỉ Vân, sơ bộ quan sát bột Tam thất, trị ho ra máu, tạp chí Trung Y 1965, 11:29).
- Trị tiểu ra máu: trị 39 ca bệnh nhân tiểu ra máu, mỗi 4-8 giờ uống bột Tam thất 0.9-1.5g, đại bộ phận bệnh nhân sau khi dùng thuốc trên dưới 3 ngày hết tiểu ra máu (khoa Tiết niệu ngoại Bệnh viện số 1 Cáp Nhĩ Tân, Quan sát lâm sàng bột Tam thất trị tiểu ra máu, báo Đại học Y Cáp Nhĩ Tân 1947, 7:51).
- Trị xuất huyết nhãn tiền phong: Do chấn thương nhãn tiền phòng xuất huyết 21 ca, trường hợp xuất huyết nhẹ, nhỏ mắt 2% dịch Tam thất, ngày 6 lần trường hợp xuất huyết nhiều ngoài việc nhỏ mắt dùng thêm phương pháp thẩm thấu ion 10% dịch Tam thất ngày 1 lần, mỗi lần 20 phút. Kết quả: trừ 1 ca xuất huyết lâu ngày teo củng mạc không kết quả, 1 ca xuất huyết giác mạc nhuộm máu kết quả không rõ, còn lại vài ngày sau hết, thị lực hồi phục nhanh (Trạm bảo vê Sức khoẻ Xưởng Điện Cơ Thượng Hải 1987, 3:16).
- Trị chấn thương sọ não:
Cho uống bột Tam thất 3g (hôn mê cho xông qua mũi) ngày 2-3 lần, theo dõi trị 40 ca, có kết quả 75% đối với thể nhẹ và vừa, kết quả tốt, ý thức hồi phục nhanh, triệu chứng thần kinh và cảm giác chủ quan được cải thiện, nước não tuỷ trong nhanh, lưu lượng máu, lực cản mạch máu và phù não đều được cải thiện. Thời gian dùng thuốc 3-10 ngày dài nhất là 21 ngày, trường hợp nặng dùng thêm thuốc lợi niệu, trụ sinh, an thần, … (Khoa Ngoại thần kinh bệnh viện thực hành số thuộc Y học viện Quảng Tây, quan sát kết quả điều trị 40 ca chấn thương sọ não điều trị bằng Tam thất, báo Tây Y học 1979, 10:330).
- Trị bệnh mạch vành:
- Dùng Tam thất quan tâm ninh (chiết xuất từ Tam thất) trong 28 bệnh viện của 7 tỉnh đã tổng kết 828 ca bệnh mạch vành mỗi ngày uống 0.6-1.2g, 778 ca đau thắt ngực có kết quả 70.2% kết quả rõ rệt 20.1% (trong tổng số liệu trình từ 4 đến 6 tháng), tỷ lệ kết quả 82.7%, 625 ca kiểm tra điện tâm đồ có kết quả 34.8%, kết quả rõ rệt 14.2% (Phóng viên báo Trung thảo dược ghi báo cáo tại Hội nghị toàn quốc tại Côn Minh về kiểm định bài thuốc “Tam thất quan tâm ninh”, báo Trung thảo dược 1980, 11:439).
- Phức Phương Tam Thất Quan Tâm Phiến, gồm: Tam thất 0.8g, Diên hồ sách 4g, Hồng hoa, Chế thủ ô, Kê huyết đằng mỗi thứ 12g, Một dược 2g. Tất cả liều đều lượng 1 ngày chia 3 lần uống. 30 ngày là một liệu trình, dùng trị 1-2 liệu trình nhận thấy kết quả: 68 ca đau thắt tim (127 lần), tỷ lệ kết quả 88.2% trước khi dùng thuốc có 52 lần (ca) đã dùng Nitroglycerin, sau khi điều trị bằng bài Phức phương tam thất có 73.1% không dùng hoặc giảm liều. Tỷ lệ có kết quả điện tâm đồ 26.7% (Tổ phòng trị bệnh mạch vành, Tổng Y viện Giải phóng quân nhân dân Trung Quốc, Quan sát kết quả điều trị bệnh mạch vành bằng “Quan tâm phiến” 68 ca, tạp chí Tân Y Dược học 1973, 10:120).
- Trị chứng tăng lipid huyết:
Tác giả dùng bột Tam thất sống cho uống 0.6g/lần x 3 lần/ngày.
- Một số bài thuốc chứa Sâm tam thất được đề cập trong dược điển:
Hiện nay, theo dược điển Trung Quốc 2020, thành phần Sâm tam thất được phối rất nhiều trong các bải thuốc cổ phương lẫn hiện đại mà ở phần tài liệu này khó mà có thể tổng hợp hết được, bạn có thể tìm hiểu thêm các bài thuốc trong dược điển Trung Quốc 2020 nếu muốn tìm hiểu sâu hơn.
Điều hoà huyết áp: Hồng hoa (Cartharni Flos) 120g, rễ Đương quy (Angelicae Sinensis Radix) 60g, Huyết rồng (Draconis Sanguis) 14g, rễ và thân rễ Sâm tam thất (Notoginseng Radix et Rhizoma) 20g, thân rễ Cốt toái bổ - đã trần (Drynariae Rhizorna .(scalded)) 60g, rễ Tục đoạn (Dipsaci Radix) 60g, Nhũ hương - đã chế biến (Olibanum ( processed)) 60g, Mộc dược - đã chế biến (Myrrha (processed)) 60g, cây cau (catechu) 40g, rễ và thân rễ Đại hoàng (Rhei Radix et Rhizoma) 40g, Băng phiến tổng hợp (Bomeolum Syntheticum) 4g, Bọ đuôi kìm (Eupolyphaga Steleophaga) 40g. Pha với nước ấm đun sôi để nguội hoặc rượu vang vàng với 3g hỗn hợp bột thuốc/lần, uống 2 lần/ngày. Để sử dụng ngoài da, thoa lên vùng bị ảnh hưởng sau khi pha trộn với giấm hoặc rượu vang vàng. Chống chỉ định cho phụ nữ có thai và cho con bú, hoặc trực tiếp lên vùng da bị thương.
Liều dùng và chú ý:
Thuốc bột 3-9g/lần, uống mỗi lần từ 1-3g, cấp có thể dùng 4-5 lần/ngày. Dùng ngoài: Lượng thích hợp. Kiêng kị phụ nữ có thai và cho con bú.
TÀI LIỆU THAM KHẢO
- Tung, B. T., & Hai, N. T. (2016). Phytochemical and pharmacology effect of Panax notoginseng. Journal of Applied Pharmaceutical Science, 6(8), 174-178. [Get link]
- Zhang, H., Li, J., Diao, M., Li, J., & Xie, N. (2024). Production and pharmaceutical research of minor saponins in Panax notoginseng (Sanqi): Current status and future prospects. Phytochemistry, 114099. [Get link]
- Ji, C., Lu, Y., Li, J., Hua, M. Z., Xie, Y., Ma, Y., ... & Lu, X. (2023). Determination of Dencichine in Panax notoginseng in the Forest and field using high performance liquid chromatography. Acs Omega, 8(30), 27450-27457. [Get link]
- Zhang, Q., Liu, G., Li, Y., Yang, B., Guo, W., Zhang, Y., ... & Kong, D. (2023). Thermal proteome profiling reveals the glial toxicity of dencichine via inhibiting proteasome. Food and Chemical Toxicology, 182, 114146. [Get link]
- Hu, Y., He, Y., Niu, Z., Shen, T., Zhang, J., Wang, X., ... & Cho, J. Y. (2022). A review of the immunomodulatory activities of polysaccharides isolated from Panax species. Journal of Ginseng Research, 46(1), 23-32. [Get link]
- Zhang, C., Zhang, B., Zhang, X., Wang, M., Sun, X., & Sun, G. (2022). Panax notoginseng saponin protects against diabetic cardiomyopathy through lipid metabolism modulation. Journal of the American Heart Association, 11(4), e023540. [Get link]
- Xu, Y., Wang, N., Tan, H. Y., Li, S., Zhang, C., & Feng, Y. (2021). Gut-liver axis modulation of Panax notoginseng saponins in nonalcoholic fatty liver disease. Hepatology international, 15, 350-365. [Get link]
- Chen, J., Li, L., Bai, X., Xiao, L., Shangguan, J., Zhang, W., ... & Liu, G. (2021). Inhibition of autophagy prevents Panax notoginseng saponins (PNS) protection on cardiac myocytes against endoplasmic reticulum (ER) stress-induced mitochondrial injury, Ca2+ homeostasis and associated apoptosis. Frontiers in Pharmacology, 12, 620812. [Get link]
- Cang, D., Zou, G., Yang, C., Shen, X., Li, F., Wu, Y., & Ji, B. (2021). Dencichine prevents ovariectomy-induced bone loss and inhibits osteoclastogenesis by inhibiting RANKL-associated NF-κB and MAPK signaling pathways. Journal of Pharmacological Sciences, 146(4), 206-215. [Get link]
- Ning, K., Jiang, L., Hu, T., Wang, X., Liu, A., & Bao, Y. (2020). ATP‐Sensitive Potassium Channels Mediate the Cardioprotective Effect of Panax notoginseng Saponins against Myocardial Ischaemia–Reperfusion Injury and Inflammatory Reaction. BioMed research international, 2020(1), 3039184. [Get link]
- Qiao, Y., Ma, Q., Li, Y., Fan, C., & Tang, M. (2020). Neuroprotective Effects of Panax Notoginseng Saponins against Cerebral Ischemia via Improving Glutamate Metabolism Pathway: In Vivo and In Vitro. [Get link]
- Liu, F., Wang, M., Wang, Y., Cao, Y., Sun, Z., Chen, M., ... & Huang, C. (2019). Metabonomics study on the hepatoprotective effect of Panax notoginseng leaf saponins using UPLC/Q-TOF-MS analysis. The American Journal of Chinese Medicine, 47(03), 559-575. [Get link]
- Shen, Q., Li, J., Zhang, C., Wang, P., Mohammed, A., Ni, S., & Tang, Z. (2017). Panax notoginseng saponins reduce high-risk factors for thrombosis through peroxisome proliferator-activated receptor-γ pathway. Biomedicine & Pharmacotherapy, 96, 1163-1169. [Get link]
- Zhao, H., Han, Z., Li, G., Zhang, S., & Luo, Y. (2017). Therapeutic potential and cellular mechanisms of Panax notoginseng on prevention of aging and cell senescence-associated diseases. Aging and disease, 8(6), 721. [Get link]
- Jie, L., Pengcheng, Q., Qiaoyan, H., Linlin, B., Meng, Z., Fang, W., ... & Siwang, W. (2017). Dencichine ameliorates kidney injury in induced type II diabetic nephropathy via the TGF-β/Smad signalling pathway. European journal of pharmacology, 812, 196-205. [Get link]
- Han, S. X., & You, Y. (2016). Balance between cardiovascular pharmacological and hemolytic effects of saponins of Panax notogenseng. Zhongguo Zhong yao za zhi= Zhongguo Zhongyao Zazhi= China Journal of Chinese Materia Medica, 41(5), 818-822. [Get link]
- Zhong, L., Zhou, X. L., Liu, Y. S., Wang, Y. M., Ma, F., Guo, B. L., ... & Zhang, Q. Y. (2015). Estrogen receptor α mediates the effects of notoginsenoside R1 on endotoxin-induced inflammatory and apoptotic responses in H9c2 cardiomyocytes. Molecular medicine reports, 12(1), 119-126. [Get link]
- Ding, R. B., Tian, K., Cao, Y. W., Bao, J. L., Wang, M., He, C., ... & Wan, J. B. (2015). Protective effect of panax notoginseng saponins on acute ethanol-induced liver injury is associated with ameliorating hepatic lipid accumulation and reducing ethanol-mediated oxidative stress. Journal of Agricultural and Food Chemistry, 63(9), 2413-2422. [Get link]
- Xu, D., Huang, P., Yu, Z., Xing, D. H., Ouyang, S., & Xing, G. (2015). Efficacy and safety of Panax notoginseng saponin therapy for acute intracerebral hemorrhage, meta-analysis, and mini review of potential mechanisms of action. Frontiers in Neurology, 5, 87859. [Get link]
- Zhou, N., Tang, Y., Keep, R. F., Ma, X., & Xiang, J. (2014). Antioxidative effects of Panax notoginseng saponins in brain cells. Phytomedicine, 21(10), 1189-1195. [Get link]
- Huang, L. F., Shi, H. L., Gao, B., Wu, H., Yang, L., Wu, X. J., & Wang, Z. T. (2014). Decichine enhances hemostasis of activated platelets via AMPA receptors. Thrombosis Research, 133(5), 848-854. [Get link]
- Liu, Z., Chen, J., Huang, W., Zeng, Z., Yang, Y., & Zhu, B. (2013). Ginsenoside Rb1 protects rat retinal ganglion cells against hypoxia and oxidative stress. Molecular Medicine Reports, 8(5), 1397-1403. [Get link]
- Shang, Q., Xu, H., Liu, Z., Chen, K., & Liu, J. (2013). Oral Panax notoginseng preparation for coronary heart disease: a systematic review of randomized controlled trials. Evidence‐Based Complementary and Alternative Medicine, 2013(1), 940125. [Get link]
- Yuan, Z., Liao, Y., Tian, G., Li, H., Jia, Y., Zhang, H., ... & Zhang, Y. (2011). Panax notoginseng saponins inhibit Zymosan A induced atherosclerosis by suppressing integrin expression, FAK activation and NF-κB translocation. Journal of Ethnopharmacology, 138(1), 150-155. [Get link]
- Xie, G. X., Qiu, Y. P., Qiu, M. F., Gao, X. F., Liu, Y. M., & Jia, W. (2007). Analysis of dencichine in Panax notoginseng by gas chromatography–mass spectrometry with ethyl chloroformate derivatization. Journal of pharmaceutical and biomedical analysis, 43(3), 920-925. [Get link]
- Chan, R. Y., Chen, W. F., Dong, A., Guo, D., & Wong, M. S. (2002). Estrogen-like activity of ginsenoside Rg1 derived from Panax notoginseng. The Journal of Clinical Endocrinology & Metabolism, 87(8), 3691-3695. [Get link]
- Lam, S. K., & Ng, T. B. (2002). Pananotin, a potent antifungal protein from roots of the traditional Chinese medicinal herb Panax notoginseng. Planta medica, 68(11), 1024-1028. [Get link]
- Lam, S. K., & Ng, T. B. (2002). A xylanase from roots of sanchi ginseng (Panax notoginseng) with inhibitory effects on human immunodeficiency virus-1 reverse transcriptase. Life Sciences, 70(25), 3049-3058. [Get link]
- Chan, P., Thomas, G. N., & Tomlinson, B. (2002). Protective effects of trilinolein extrated from Panax notoginseng against cardiovascular disease. Acta Pharmacologica Sinica, 23(12), 1157-1162. [Get link]

